一种抗癌“神药”——阿司匹林
发布日期:2023-11-15 浏览次数:9659
西班牙哲学家加塞特曾在他的书中写道:“阿司匹林是文明带给人类的惠赠“。如此盛赞,不是过誉,而是写实。
01 “老药“再发新枝
阿司匹林,又名乙酰水杨酸,可以说是一种“古老”的药物。
图一 阿司匹林的分子结构式
1897年,德国化学家霍夫曼将水杨酸与醋酐进行反应,从而合成出乙酰水杨酸。1899年3月6日,阿司匹林的发明专利审批通过,随后其临床试验也很快取得了成功,德国拜耳药厂正式生产该药品,并将商品命名为Aspirin(阿司匹林)。阿司匹林主要用作解热镇痛、非甾体抗炎药,抗血小板聚集药。在近百年的临床应用历史上,它所使用的范围颇广:最初人们用它抑制炎症、解热,最新的基础研究显示,阿司匹林还能够提高认知功能,预防阿尔茨海默症!而且,研究人员发现,阿司匹林“老药新用“的潜力仍然很大。
02 阿司匹林如何抗癌
2007年,在一篇系统性的综述中,阿司匹林被报道能够降低结直肠癌的风险,随后引发了一系列关于阿司匹林能否抑制肿瘤的研究。
2018年,《JAMA Oncology》发表的由麻省总医院(MGH)领衔的一项研究表明,长期服用阿司匹林可以降低HCC发病风险,并且随着服用剂量增加和时间延长,风险逐步下降(1)。2020年,NEJM发表的一项研究发现,服用低剂量(<=160mg/ day)的阿司匹林与肝癌风险降低31%,相关死亡风险降低27%相关(2)。目前,基础研究所解析的阿司匹林抗癌机制主要集中在抑制血小板活化,抑制细胞增殖。
今年,来自复旦大学基础医学院的研究团队发现了阿司匹林抗癌的新机制:通过调控免疫检查点分子FGL1的乙酰化修饰(3)。我们知道,肿瘤细胞非常聪明,他们会通过不同的策略躲避机体免疫系统的监视。在这些策略中,最为经典的、曾获得过诺贝尔奖的例子是,肿瘤细胞会促发PD-L1/PD-1免疫抑制通路。肿瘤细胞会故意上调免疫抑制性配体PD-L1与T细胞表面的PD-1相结合,以此降低T细胞的攻击能力。当然,除了这一条“鸡贼”的策略,肿瘤细胞还有其他小花招,比如后文将会介绍的FGL1/LAG-3免疫抑制通路。
图二 T细胞上的PD-1和肿瘤细胞上的PD-L1结合(图片来源网络)
那么,什么是蛋白质的乙酰化修饰呢?
蛋白质的乙酰化修饰是蛋白质翻译后修饰的其中一种重要类型,它就像是蛋白质的小马甲——当一个蛋白穿上运动服,他就要去健身房撸铁;当这个蛋白脱下运动服换上西装,便成了文质彬彬的上班族;当这个蛋白质换上居家服,说不定就是在家跪搓衣板了。也就是说,乙酰化修饰赋予目的蛋白不同场合下的不同角色,有些蛋白质穿上乙酰化这件衣服会从“细胞质”去隔壁的“细胞核”串门,有些蛋白质穿上乙酰化修饰会被死神带走,去到“火葬场”蛋白酶体进行灭口,而有些蛋白质穿上乙酰化修饰则束手束脚,受到压制,变得不再像平时那般雷厉风行。
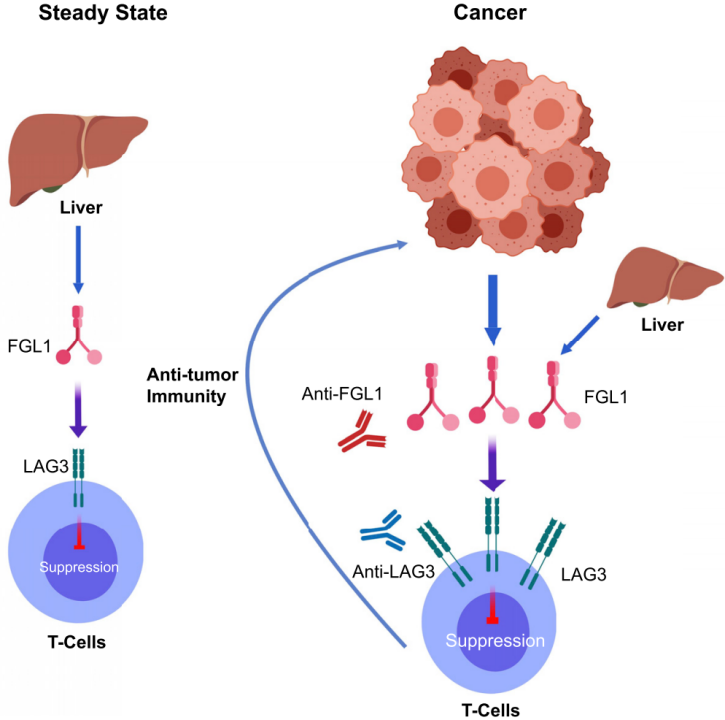
图三 T细胞上的LAG-3和肿瘤细胞的FGL1结合(4)
2019年,耶鲁大学的免疫学专家陈列平教授的团队率先发现,一种叫FGL1的蛋白分子是T细胞表面免疫受体LAG-3的特异性免疫配体(图三)。当阻断FGL1与LAG-3之间的结合则能够促进免疫治疗的效果,该结论在包括肺癌,肝癌在内的小鼠模型中得到了初步验证(4)。因此,靶向FGL1蛋白分子是一种潜在的提高免疫治疗效果的策略。复旦大学研究团队发现,阿司匹林能够直接将自己的活性乙酰基团强行穿在FGL1蛋白上,导致FGL1蛋白被拉到细胞质的垃圾桶“蛋白酶体”中灭口。体外的实验结果表明,使用阿司匹林对肿瘤细胞进行预处理能够恢复共培养体系中的T细胞的活性。体内实验结果进一步证实,联合使用阿司匹林和PD-L1单克隆抗体能够有效地抑制肝癌小鼠肿瘤的生长,并且延长小鼠的生存期。
03 能不能自行服用阿司匹林
众所周知,所有抗癌药物都要经过大量的前期基础研究和严格的临床试验,以确定科学的用药剂量和最佳的给药方式。上述提到的多项关于阿司匹林抗癌的研究都属于临床前的基础研究,在小鼠的体内模型中验证了阿司匹林能够抑制肿瘤。这些数据为免疫治疗方案的临床评估提供了动力,但是考虑到阿司匹林抗癌功效的部分负面结果,是否在治疗中联用阿司匹林应当经过医生的谨慎考虑,病人应当在遵循医嘱的情况下服用药物并进行密切观察。因此,阿司匹林是否能够联合现有的免疫检查点抑制剂药物成为癌症治疗的临床方案依然有待时间的考察。
展望未来,将会有越来越多关于阿司匹林的相关研究成果,其潜在的作用机制也将被挖掘出来,给人类抗癌带来更多的希望。
参考文献:
1. Simon TG, Ma Y, Ludvigsson JF, Chong DQ, Giovannucci EL, Fuchs CS, et al. Association Between Aspirin Use and Risk of Hepatocellular Carcinoma.Jama Oncol. 2018;4(12):1683-90.
2. Simon TG, and Ludvigsson JF. Association between Aspirin and Hepatocellular Carcinoma. Reply. N Engl J Med. 2020;382(25):2481-2.
3. Lin M, He J, Zhang X, Sun X, Dong W, Zhang R, et al. Targeting fibrinogen-like protein 1 enhances immunotherapy in hepatocellular carcinoma. J Clin Invest. 2023;133(9).
4. Wang J, Sanmamed MF, Datar I, Su TT, Ji L, Sun J, et al. Fibrinogen-like Protein 1 Is a Major Immune Inhibitory Ligand of LAG-3. Cell.2019;176(1-2):334-47 e12.
作者简介
林铭恩、吕雷
代谢分子医学教育部重点实验室
复旦大学基础医学院生物化学与分子生物学系